|
Papierchromatographie Wegen ihrer Einfachheit war die Papierchromatographie eine weit verbreitete
Technik zur Analyse von Stoffgemischen. Für die medizinische Labordiagnostik hat sie nur
mehr historische Bedeutung.
 |
Schema des Ablaufs einer absteigenden Papierchromatographie 1. Auf einem Papier wird das Probengemisch aufgetragen. Dann
wird das Ende des Papierstreifens in eine Wanne gehängt, in der sich die mobile Phase
(eine Flüssigkeit) befindet.
2. Die mobile Phase wandert durch Kapillarwirkung
und Schwerkraft den Papierstreifen entlang. Die einzelnen Stoffe der Probe nimmt sie dabei
verschieden weit mit.
Nach der Trennung entnimmt man das Papier und trocknet es.
|
Ergänzungen zur Abbildung: Es wäre schlecht,
wenn die mobile Phase vom Papier weg verdunstet. Damit das nicht passiert, lässt man die
Papierchromatographie in einem geschlossenen Behälter ablaufen, in den etwas mobile Phase
eingefüllt wird, die den Boden bedeckt. Die Luft ist dann mit der mobilen Phase
gesättigt. Während die Chromatographie läuft, hängt die links oben dargestellte
Anordnung in diesem Behälter (ohne den Boden zu berühren).
Es gibt auch eine aufsteigende Papierchromatographie. Die ist apparativ ein wenig
einfacher. Man füllt in einen Behälter wenige Zentimeter hoch mobile Phase und hängt
das Papier so hinein, dass es in diese eintaucht. Der Nachteil ist, dass die Trennung
gegen die Schwerkraft erfolgt und die Laufstrecke maximal etwa 30 cm lang wird. Länger
Laufstrecken bedeuten aber höher auflösende Trennungen. |
Auf welchem Prinzip beruht die Trennung bei
der Papierchromatographie?
- Stationäre Phase
Die stationäre Phase bildet der Wassermantel, der die Zellulosefasern umgibt.
|
Zellulose, hat verschiedene Eigenschaften, die es als
Trägermaterial für die Chromatographie geeignet machen:
- Die einzelnen Zellulosefasern bilden ein Geflecht, das
durchlässig ist und eine große Oberfläche bietet.
- Zellulose hat die Eigenschaft Wasser anzuziehen. Die
Zellulosefasern sind daher von einem Wassermantel umgeben.
|
- Mobile Phase
Als mobile Phase eignen sich organische Lösungsmittelflüssigkeiten, z.B. Butanol oder
Phenol.
(Diesen muss Wasser beigemischt werden, damit sie beim Durchwandern des Papiers
diesem nicht seinen Wassermantel entziehen).
- Der Trennungsmechanismus
Die Trennung beruht bei der Papierchromatographie vorwiegend auf einer Verteilungs-Chromatographie.
Die Stoffe verteilen sich zwischen der wässrigen stationären Phase und der Flüssigkeit
der mobilen Phase. Stoffe, die sich gut in Wasser lösen, bleiben länger in der
stationären Phase und werden nur langsam wandern. Stoffe die besser in der mobilen Phase
löslich sind wandern schnell.
Wie macht man das Ergebnis sichtbar?
Trennt man Farbstoffe, ist es leicht. Sie bilden farbige Flecken.
Ungefärbte Stoffe, die fluoreszieren, kann man im UV-Licht sichtbar machen. Radioaktive
Stoffe können eine Photoplatte schwärzen. Andere Stoffe muss man mit einem
aufzusprühenden Nachweisreagenz einfärben.
Woher weiß man welcher "Fleck"
welcher Substanz entspricht?
Das ist tatsächlich nicht immer so einfach. Prinzipiell erkennt man
Substanzen (=Stoffe) in der Chromatographie daran, wie schnell sie laufen. Also bei der
Papierchromatographie an der Strecke, die sie zurückgelegt haben. Und zwar am einfachsten
im Vergleich zur Front der mobilen Phase.
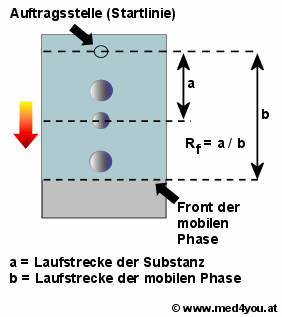 |
Berechnung des Rf-Wertes
Dividiert man die Laufstrecke der Substanz (a) durch die der mobilen Phase (b), erhält
man den sog. Rf-Wert.
Dieser Wert (er liegt zwischen 0 und 1) ist für jeden Stoff bei gleichbleibenden
Bedingungen charakteristisch. Er dient daher der Erkennung der Stoffe. Leider können
verschiedene Stoffe gleiche Rf-Werte haben.
Die Abkürzung Rf wird mit "relate
to front" aber auch mit "ratio front"
erklärt. |
Als Alternative oder als zusätzliche Maßnahme kann
man auch eine bekannte Substanz als Standard mitlaufen lassen:
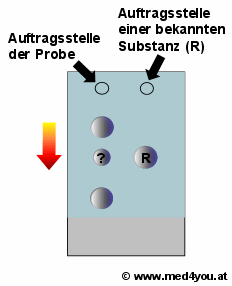 |
Parallele Analyse einer Standardsubstanz
Man trägt neben der Probe eine bekannte Substanz auf, die als Referenz-Standard dient
(R). Die fragliche Substanz (?) hat die gleiche Wanderungsstrecke und könnte mit dem
Standard ident sein.
Außerdem kann man für jeden Fleck die sog. RST-Werte berechnen. Der RST-Wert
ist die Laufstrecke einer Substanz der Probe dividiert durch die Laufstrecke des
Standards. Auch dieser Wert kann helfen zu erkennen, welche Substanz den Fleck auf dem
Papier verursacht hat.
Die Abkürzung RST wird mit "relative
to standard" aber auch mit "ratio standard"
erklärt. |
Wie kann man die Stoffe quantifizieren (die
Menge bestimmen)?
Ein Anhaltspunkt für die Menge ist die Größe des Flecks. Man hat
früher mit Millimeterpapier die Fläche abgemessen und daraus die Menge berechnet (sie
ist proportional zum Logarithmus der Fläche). Man hat Flecken auch ausgeschnitten um die
Menge des Stoffs zu bestimmen.
Heute kann man das Ergebnis mit dem Computer einscannen und die Fläche und Konzentration
berechnen lassen.
Das sind aber alles keine idealen Methoden und das ist auch einer der Nachteile der
planaren Chromatographien (Papier- und Dünnschichtchromatographie): Man kann die Menge
der aufgetrennten Stoffe nur sehr schwer und nur ungenau bestimmen.
Zweidimensionale Papierchromatographie
Wenn man eine "fertige" Papierchromatographie um 90°
dreht und in eine andere mobile Phase taucht, kann man die Stoffe ein 2. Mal auftrennen.
Flecken, die nach der ersten Trennung einheitlich schienen, können sich nach der zweiten
Trennung in zwei oder mehrere Flecken aufteilen. Das weist darauf hin, dass der
ursprüngliche Fleck von mehr als einem Stoff verursacht wurde.
Anwendungen der Papierchromatographie
Wie erwähnt, wird die Papierchromatographie heute kaum noch
eingesetzt, Früher verwendete man sie u.a. zum Nachweis von Aminosäuren im Harn,
Nachweis von Medikamenten und zur Identifikation von Zuckern.
|
|
|
Dünnschichtchromatographie Die Dünnschichtchromatographie ist ein Verfahren zur Auftrennung und Analyse
von Stoffgemischen. Sie gehört wie die Papierchromatographie zu den planaren
Chromatographien (Flachbett-Chromatographien). Die beiden Methoden haben sehr viel
gemeinsam und ein großer Teil des für die Papierchromatographie Gesagten gilt auch für
die Dünnschichtchromatographie. Die nachfolgenden Informationen beschränken sich daher
auf das Wesentlichste und auf die Unterschiede zwischen den beiden Methoden.
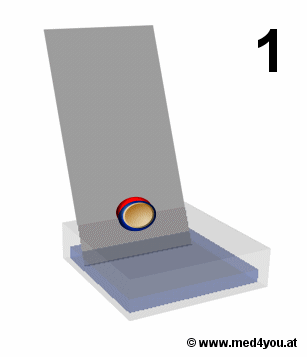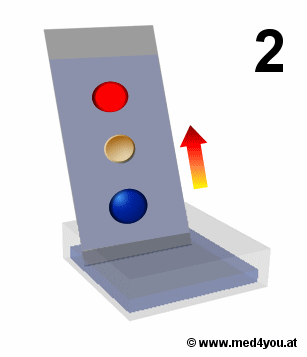 |
(Aufsteigende) Dünnschichtchromatographie
Die Dünnschichtplatte wird in die mobile Phase getaucht. Die mobile Phase steigt hoch.
Stoffe werden getrennt, weil sie von der mobilen Phase verschieden weit mitgenommen
werden.
Ergänzung zur Abbildung: Auch die Dünnschichtchromatographie muss in einer
Entwicklungskammer laufen, also in einem verschlossenen Behälter. So ist die Luft mit
mobiler Phase gesättigt und diese verdunstet nicht von der Dünnschichtplatte weg. |
Auf welchem Prinzip beruht die Trennung bei
der Dünnschichtchromatographie?
- Stationäre Phase
Die stationäre Phase wird von einer dünnen Schicht einer stark adsorbierenden Substanz
gebildet. In der ursprünglichen Form wurde diese Schicht auf eine Glasplatte aufgebracht.
Die vorwiegend verwendeten Adsorbentien sind Siliziumoxide (Kieselgur, Kieselgel),
Magnesiumsilicat, Magnesiumoxid und Aluminiumoxid.
Prinzip der Herstellung: Man verrührt die Adsorbentien mit destilliertem Wasser zu
einem Brei, trägt diesen gleichmäßig auf die Platte auf und lässt sie Hitze-trocknen.
Heute werden aber nur fertige Produkte verwendet.
- Mobile Phase
Als mobile Phase eignen sich organische Flüssigkeiten (z.B. Petrolether, Isopropanol,
Butanol o.Ä.).
- Der Trennungsmechanismus
Die Trennung beruht bei der Dünnschichtchromatographie vorwiegend auf Adsorptionsphänomenen. Die
Stoffe verteilen sich zwischen der Oberfläche der stationären Phase und der Flüssigkeit
(mobilen Phase).
Für die Wanderungsgeschwindigkeit (bzw. Laufstrecke) entscheidend ist:
- Wie stark bindet sich der Stoff an die stationäre Phase, an das
Adsorbens.
- Wie gut ist der Stoff in der mobilen Phase löslich.
Stoffe, die stark an die stationäre Phase binden und/oder schlecht in der mobilen
Phase löslich sind, bleiben länger an der stationären Phase hängen und werden nur
langsam wandern. Stoffe die sich weniger stark anlagern und/oder gut in der mobilen Phase
löslich sind wandern schnell.
Bezüglich Sichtbarmachen, Identifikation und
Quantifizierung der aufgetrennten Stoffe siehe unter Papierchromatographie.
Vergleich Dünnschichtchromatographie /
Papierchromatographie
Die Dünnschichtchromatographie zeigt:
- bessere Auftrennung der Stoffe,
- schnellere Auftrennung,
- robuste stationäre Phase und robuster Träger (d.h., man ist in der
Auswahl der Nachweisreagenzien ziemlich frei).
- verschiedene stationäre Phasen verwendbar
Durch Weiterentwicklungen in der Dünnschichtchromatographie (siehe
nächster Punkt) weist sie keine entscheidenden Nachteile mehr auf.
Breites Spektrum am Markt
Hier wurde die klassische Dünnschichtchromatographie beschrieben.
Es gibt aber inzwischen zahlreiche Varianten, die alle unter dem Begriff
Dünnschichtchromatographie laufen, sich aber von der ursprünglichen Form deutlich
unterscheiden.
- Flexible Träger
Das Adsorbens wird statt auf Glasplatten auf flexible Kunststofffolien aufgebracht. So
muss man den Stoff nach der Trennung nicht abkratzen, um ihn zu gewinnen, sondern kann ihn
wie bei der Papierchromatographie ausschneiden.
- High Performance Thin Layer Chromatography (HPTLC)
Durch Verwendung von Adsorbentien mit besonders kleiner Partikelgröße kann man Stoffe
besser auftrennen, daher "high performance" (hohe Leistung). "Thin Layer
Chromatography" ist Englisch für Dünnschichtchromatographie.
- Reversed-Phase Thin Layer Chromatography (RP-TLC)
Man kann auf die Adsorptionsmaterialien eine Schicht Kohlenstoffketten auftragen. Dadurch
erhält man eine stationäre Phase, an die apolare Stoffe stark binden (hydrophobe Phase).
Die mobile Phase kann dann polar (hydrophil) sein. Da das eine Umkehrung der klassischen
Verhältnisse der Phasen ist, spricht man von "reversed
phase"-Dünnschichtchromatographie oder seltener von Umkehr-Phasen Dünnschichtchromatographie.
Anwendungen der Dünnschichtchromatographie
Im medizinischen Routinelabor wird die Methode kaum noch eingesetzt.
Manche Labors weisen damit Drogen oder Porphyrine im Harn nach (Porphyrine treten bei
bestimmten Stoffwechselkrankheiten vermehrt auf). Spezialisierte Labors verwenden die
Dünnschichtchromatographie auch zum Nachweis von seltenen Stoffwechseldefekten beim
Neugeborenen.
Vergleich Dünnschichtchromatographie /
Säulen-Chromatographie (HPLC, GC)
Die moderneren Verfahren wie HPLC und GC haben sich auf Grund ihrer
deutlich höheren Leistungsfähigkeit und erweiterten Möglichkeiten durchgesetzt. Die
Dünnschichtchromatographie wird in der Routineanalytik kaum noch verwendet. Sie hat aber
auch Vorteile, die bei speziellen Anwendungen eine Rolle spielen können: Niedriger
apparativer Aufwand, niedrige Kosten, einfache Durchführung, relativ robust gegenüber
"verschmutzten" Proben. Mehrere Proben in einem Lauf analysierbar. |
|




